深圳子科生物報道:11月13日,清華醫學院生物醫學工程系杜亞楠研究組于學術期刊《自然·材料學》(Nature Materials)在線發表了題為“基于體外仿生肝纖維化3D病理模型研究肝臟血管新生促進纖維化的生物力學機制和干預策略”(Mechanotransduction-modulated fibrotic microniches reveal the contribution of angiogenesis in liver fibrosis)的研究長文。該研究創新性地構建了模擬肝臟纖維化病理發展從早期到晚期不同階段的體外仿生3D微環境模型,報道了肝竇毛細血管過程中通過膠原纖維傳遞的機械力學刺激信號在促進肝臟纖維化發展中的作用和機制,并且進一步針對性地提出了抗肝臟纖維化的干預策略(圖1)。

圖1:基于膠原纖維機械力學介導的血管新生促進肝臟纖維化發病機制和干預概念圖。
我國是肝病大國,肝炎、非酒精脂肪肝和酒精肝等肝臟疾病影響了約3億人的健康。肝纖維化是上述慢性肝病發展到肝硬化的必經階段,有關資料顯示我國約有500-700萬肝硬化患者,且發病人數逐年升高,zui終可導致肝癌。我國每年約40萬人死于肝癌,是第二大致死癌癥,占世界肝癌死亡人數的一半。此前臨床研究和動物模型中,均發現血管新生伴隨肝臟纖維化發生的現象,然而學術界對于血管新生與纖維化之間的關系及相互作用機理尚不清晰,同時在臨床前研究中抗血管藥物對于逆轉肝纖維化的療效也存在爭議。
這項研究通過臨床樣本和疾病動物模型發現血管新生在肝臟纖維化早期大量發生而在晚期較少發生,提示其作用機制存在病理階段特異性。據此病理現象,研究團隊基于機械力調控構建了模擬肝臟纖維化不同發展階段的仿生3D肝臟纖維化微環境(Fibrotic microniches, FμNs),探究了肝纖維化發展不同階段肝竇內皮細胞(血管新生效應細胞)與肝星型細胞(纖維化效應細胞)的相互作用。
研究人員基于纖維化微環境,發現了血管新生促進肝纖維化發生的病理階段特異性,并報道了“早期肝纖維化階段肝竇毛細血管新生重塑的膠原纖維可作為機械力傳導介質直接激活星型細胞”這一生物力學現象和相關分子機制。基于此發現進一步提出了靶向血管新生治療肝臟纖維化的治療方案。
研究團隊還結合微加工技術,將此肝纖維化微環境模型進一步微小化為含有384個纖維化微環境微單元的藥物篩選陣列,形成高通量體外藥物檢測及篩選平臺。根據肝臟纖維化微環境體外藥敏測試,研究團隊證明了抗血管生成藥物(如索拉非尼和血管內皮生長因子抗體)僅對小鼠早期肝纖維化治療有效,而對于晚期纖維化逆轉無效;同時證明膠原重塑劑(如BAPN)可減輕晚期肝纖維化,提示靶向微環境基質組分對于晚期肝纖維化的潛在療效。
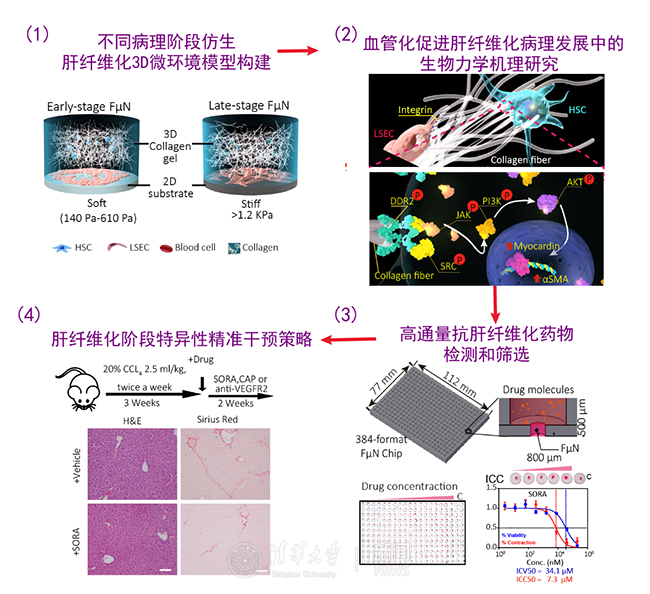
圖2 研究成果簡介:構建了模擬肝臟纖維化病理發展從早期到晚期不同階段的體外仿生3D微環境模型(1),報道了肝竇毛細血管新生過程中通過膠原纖維傳遞的機械力學刺激信號在促進肝臟纖維化發展中的作用和機制(2),并且通過高通量藥物檢測和篩選(3) 進一步針對肝纖維化病理階段特異性提出抗纖維化的干預治療方案(4).
研究提出基于膠原纖維機械力學介導的肝纖維化發病機制,并建立了相關病理和藥物篩選平臺,為肝臟纖維化治療提供了針對特定病理階段和微環境組分的干預策略,并為抗纖維化藥物篩選提供了創新理論和平臺技術(圖2)。
醫學院長聘副教授杜亞楠為本論文的通訊作者,杜亞楠研究組2013級聯合培養項目(PTN)博士生劉龍偉和2015級生物醫學工程系博士生尤志峰為本文的共同*作者。
清華大學醫學院石彥教授,夏鐵副研究員在原子力顯微鏡力學表征方面提供了。天津第二人民醫院的侯偉博士和北京清華長庚醫院黃晨昱博士對該研究的臨床意義和應用提供了支持。杜亞楠研究組的碩士生于鴻升和博士生周律、鄢曉君、趙輝、王冰潔、朱路參與了本項研究。本研究得到了國家自然科學基金委青年科學基金和國家重點研發計劃的資金資助。




